文 | 菠萝
胃癌首个一线免疫治疗方案
胃癌是中国第二大常见癌症类型。
由于幽门螺杆菌感染,高盐腌制食物摄入过量等原因,中国胃癌患者占了全球40%以上!长期以来,由于通常发现得晚,而且缺乏新药,中国胃癌患者的死亡率很高,晚期患者平均生存期不到一年。
好消息是,随着免疫治疗,靶向治疗的出现,加上胃癌预防筛查的普及,这个情况有望得到改善。
2021年4月有个里程碑事件,就是美国FDA批准了纳武利尤单抗(O药)与化疗联用一线治疗晚期或转移性的上消化道肿瘤,包括胃癌/胃食管结合部癌/食管腺癌。值得关注的是,这次的批准没有限定PD-L1和HER-2的表达情况。
这是FDA批准的首个胃癌一线免疫治疗方案,标志着胃癌一线免疫治疗时代的到来。对于符合条件的胃癌患者,单独化疗不再是唯一的选择。

此次获批背后的依据,是代号为CheckMate -649的大型III期试验。结果显示,在标准化疗方案中加入O药,HER2阴性的胃癌患者能显著获益。
研究的主要终点,是PD-L1表达阳性且CPS ≥5患者的总生存期(OS)和无进展生存期(PFS)。O药+化疗的免疫组合组取得完胜。免疫组合的中位OS为14.4个月,而化疗组是11.1个月;免疫组合组的中位PFS为7.7个月,化疗组为6.0个月。
CPS(Combined Positive Score,综合阳性分数),是用来描述肿瘤样本表达PD-L1蛋白水平的一个指标。简单地说,CPS分数越高,说明肿瘤样本里表达PD-L1的细胞越多。
毫无疑问,PD-L1 CPS ≥5患者能从免疫组合疗法中获益。但这次为什么FDA没有限定呢?因为分析数据后,发现其他患者也可能获益。
单独分析PD-L1表达阳性且CPS ≥1的患者,免疫组合的中位OS为14.0个月,而单独化疗组为11.3个月。
即使看所有入组人群,不考虑PD-L1表达,免疫组合的中位OS依然是13.8个月,而单独化疗组11.6个月。
因此,PD-L1表达量看起来并不能准确预测免疫组合疗法的效果,各个人群都可能获益。正因为如此,FDA批准了泛胃癌人群的免疫组合疗法,这点和肺癌中免疫+化疗的组合类似。
最新的中国数据
我们最关心的是,中国患者能从中获益么?
这个问题非常重要,因为胃癌和食管癌的异质性都特别高,中国和西方患者整体的生物学和临床的特性差别很大,无论是基因突变、免疫特性、幽门螺杆菌阳性率、治疗响应上都存在显著差异。
因此,虽然免疫组合疗法在国际多中心研究中取得成功,它到底适不适合中国患者,是需要数据来证明的。
为了解决这个问题,CheckMate -649研究中专门招募了200多名中国的胃癌(包括胃食管连接部癌)患者,其中包含了中国常见的各种胃癌亚型。
在最近落幕的2021年美国癌症研究协会(AACR)年会上,消化道肿瘤大咖沈琳教授和来自中国的研究者们公布了中国患者的数据。最重要的一个结论,就是中国胃癌患者也能从免疫一线治疗中获益。

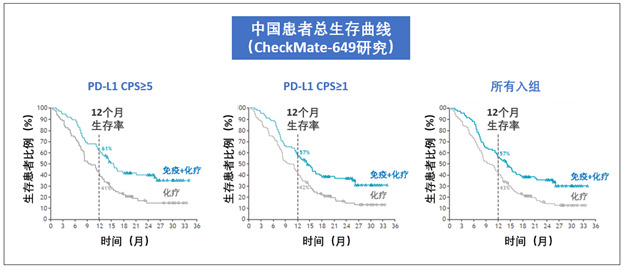
患者生存曲线和国际研究的数据类似。无论是单独分析PD-L1 CPS≥5患者,PD-L1 CPS≥1患者,还是所有入组患者,在化疗中加入免疫药都带来了生存获益。
从下面曲线能看出,无论是曲线形状,还是比较一年生存率的话,各个亚组很接近。
- PD-L1 CPS≥5患者一年生存率是61%
- PD-L1 CPS≥1患者一年生存率是57%
- 所有入组患者一年生存率是57%
都显著优于化疗的41%~43%。
除此之外,中位无进展生存期和客观缓解率等关键数据,免疫组合疗法也都显著优于化疗。
随着这些数据的公布,我相信O药+化疗的联合方案在中国也会很快获批胃癌一线治疗,也很可能没有PD-L1表达量的要求。
因为CheckMate-649研究的优秀数据,近期发布的2021年中国临床肿瘤学会(CSCO)胃癌指南中,免疫治疗也首次进入中国胃癌的一线用药推荐!
纵观这几年的中国晚期胃癌治疗指南,能明显看出。免疫治疗地位越来越高,覆盖范围也越来越大,从三线治疗迅速升级到一线。
我相信,这只是个开始。随着后续研究的深入,我们应该还能探索出更多的免疫治疗使用方法,无论是新的免疫药物,还是新的组合疗法。
而且不止是免疫治疗,胃癌还有很多新进展让人欣喜。
对于HER2阳性患者,有针对HER2的靶向药,包括新型的HER2抗体偶联药。就在这两天,美国FDA有条件批准了K药与曲妥珠单抗和化疗联用,一线治疗局部晚期不可切除或转移性HER2阳性胃癌或胃食管连接部(GEJ)腺癌患者。
对FGFR2阳性患者,有针对FGFR2的抗体药物,对于CLDN18.2阳性患者,有针对CLDN18.2的抗体药和CAR-T细胞疗法等。
这些新型疗法在各自临床研究中都获得了成功,应该都会逐步上市。胃癌的精准医疗时代,已经到来。相信随着更多创新疗法的出现,越来越多胃癌将不再是绝症,而成为能长期共存的慢性病。
当然,我经常说预防>筛查>治疗。最希望的,还是大家都能规避风险因素,并做好筛查,尽量避免晚期胃癌,保护自己和家人的健康。
致敬生命!
*本文旨在科普癌症新药背后的科学,不是药物宣传资料,更不是治疗方案推荐。如需获得疾病治疗方案指导,请前往正规医院就诊。
转自:https://mp.weixin.qq.com/s/e_rSAalAaBEr_2MPhlrOGQ